Ignacio Mártil
Catedrático de Electrónica de la Universidad Complutense de Madrid y miembro de la Real Sociedad Española de Física
[Con motivo la concesión del Premio Nobel de Química de este año a los Profesores Akira Yoshino, M. Stanley Whittingham y John B. Goodenough, por la invención y el desarrollo de las baterías recargables de iones de litio, dedicaré un par de artículos a describir las características y funcionamiento de estas baterías. En este primero describo las características esenciales de estas baterías]
 Los científicos premiados con el Nobel de Química 2019. Fuente: nobelprize.org
Los científicos premiados con el Nobel de Química 2019. Fuente: nobelprize.org
Nuestra forma habitual de comunicarnos (teléfono móvil) y cada vez más, de desplazarnos (patinetes, vehículos eléctricos, híbridos, etc.) depende del adecuado funcionamiento de un elemento que proporciona la energía necesaria para el funcionamiento de todos los dispositivos indicados: la batería recargable. Dentro de esta categoría, las baterías de iones de litio (en lo que sigue ion-litio) es, sin lugar a dudas, un dispositivo que recibe ingentes inversiones en I+D con objeto de aumentar su duración, reducir su peso y rebajar su precio. Los grandes fabricantes de teléfonos móviles y las compañías fabricantes de vehículos eléctricos, están invirtiendo fuertes sumas de dinero en el desarrollo de la siguiente generación de baterías de ion-litio de altas prestaciones.
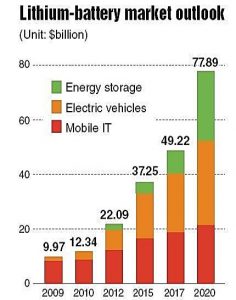
Las expectativas del mercado de estas baterías son extraordinarias. La siguiente imagen muestra la evolución prevista de estos dispositivos en sus tres principales aplicaciones: sistemas de almacenamiento de energía (el más famoso de estos es el de las célebres baterías Powerwall/Powerback de Tesla, sin olvidar las numerosas opciones que comercializan otras empresas), vehículo eléctrico y telefonía móvil:
Evolución y perspectivas para el período 2010-2020 del mercado de las baterías de ion-litio, expresado en miles de millones de dólares USA. Fuente: Lithium-battery market outlook.
En este artículo y en uno posterior voy a describir diversos aspectos de las baterías recargables. Es este analizaré las limitaciones de las baterías convencionales, cómo son las baterías recargables; qué aportan, dentro de esta categoría, las de ion-litio, para finalizar con algún detalle de una de sus aplicaciones esenciales: las baterías de los vehículos eléctricos.
1. El problema de las baterías ordinarias.
El concepto básico que explica el funcionamiento de una pila-batería (utilizo indistintamente ambos términos para referirme a estos elementos), tanto recargable como no recargable, es común a todas: al conectar cualquier dispositivo a una pila, se produce en su interior una reacción electroquímica que produce energía eléctrica. Esta idea fue descrita hace más de dos siglos por el físico italiano Alessandro Volta y desde entonces, los científicos han optimizado y mejorado el diseño original de Volta para fabricar pilas de una gran variedad de materiales y formas, siendo las más frecuentes en la actualidad las denominadas pilas alcalinas, que toman su nombre del hecho de tener uno de sus elementos clave, el electrolito, hecho de un compuesto alcalino, el KOH (hidróxido potásico).
Cuando se conectan los terminales de la pila a un electrodoméstico (una bombilla, un receptor de radio, etc.), comienzan en el interior de la pila unas reacciones químicas, por medio de las cuales los compuestos y elementos químicos que se encuentran dentro de la batería se combinan entre ellos para crear nuevos compuestos; en las reacciones, se generan partículas cargadas positivamente llamadas iones y otras cargadas negativamente, los electrones. Los iones se mueven a través del electrolito de la batería, mientras que los electrones circulan por el circuito al que está conectada la pila, proporcionando la energía eléctrica que enciende la bombilla o el receptor de radio.
El principal problema es que las baterías ordinarias no son recargables, esta reacción química puede ocurrir solo una vez y en una sola dirección. Es decir, las baterías habituales, como las alcalinas, no pueden volver a utilizarse una vez que se han descargado, porque las reacciones químicas que generan la energía no son reversibles.
2. Células de baterías recargables: conceptos esenciales
Aunque pueden adoptar diversas geometrías, en numerosas ocasiones el aspecto de las baterías-pilas recargables es prácticamente idéntico al de las pilas cilíndricas convencionales AA, aunque también se encuentran en el mercado pilas con formas prismáticas, lo que significa que son cuadradas o rectangulares. Antes de pasar a describir las pilas de ion-litio, voy a dar unos breves detalles de cómo son las baterías recargables.
Igual que las convencionales, las baterías recargables tienen una carcasa metálica que encierra y protege a sus elementos constitutivos. Ese recubrimiento contiene en su interior una espiral muy larga que está integrada por hojas delgadas muy próximas entre sí, integradas por cuatro elementos, comunes en disposición, aunque no en composición a los de cualquier otra batería:
-
-
-
-
- Un electrodo positivo, denominado cátodo
- Un electrodo negativo, el ánodo
- Un disolvente químico llamado electrolito entre ellos y
- Un separador.
-
-
-
En las baterías que no utilizan iones de litio, estos electrodos están hechos de una diversidad de compuestos químicos:
- Plomo-ácido: con dos electrodos de plomo (sulfuro de plomo o PbSO4) y electrolito de ácido sulfúrico (So4H2). Son muy baratas y fáciles de fabricar, pero contaminantes, pesadas y con baja densidad de energía (30 Wh/kg). Se utilizan sobre todo en automoción y sistemas fotovoltaicos.
- Ni-Fe: Tienen electrodos de acero niquelado y un electrolito liquido de hidróxido de potasio (KOH) disuelto en agua. Sus ventajas son similares a las de plomo-ácido, pero no contienen metales pesados, su vida es más prolongada y el electrolito se puede reciclar. Su densidad de energía también es baja, del orden de 40 Wh/kg.
- Ni-Cd: El cátodo es de hidróxido de níquel, el ánodo de cadmio y el electrolito de KOH. Su densidad de energía sigue siendo baja, unos 50 Wh/kg.
- Ni-MH: El ánodo es de hidróxido de níquel y el cátodo de una aleación de hidruro metálico. Su densidad de energía es algo más elevada, 80 Wh/kg.
Como se puede apreciar, un rasgo común a casi todas ellas es la presencia en su interior de elementos pesados, que en la mayoría de las ocasiones son tóxicos, algo especialmente crítico en el caso del plomo o el cadmio.
3. Celdas o pilas de baterías de ión-litio
Como en el caso de las baterías descritas en el punto anterior, las de ion-litio tienen un recubrimiento exterior de metal, que ahora es particularmente importante porque la batería está presurizada. Esta caja de metal tiene un orificio de ventilación sensible a la presión. Si la batería se calienta tanto que corre el riesgo de explotar debido a una sobrepresión, esta ventilación se encarga de liberar la presión generada en el interior de la pila. El respiradero está colocado como medida de seguridad. También dispone un dispositivo que evita que la batería se sobrecaliente.
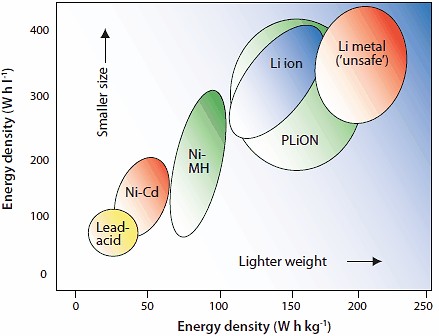
En las pilas de ion-litio, el cátodo generalmente está hecho de un compuesto químico llamado óxido de litio-cobalto (LiCoO2) o, en baterías más nuevas, de fosfato de litio y hierro (LiFePO4), para evitar utilizar cobalto, un elemento químico caro y escaso. El ánodo generalmente está hecho de grafito, una de las variedades cristalográficas del carbono. Dentro de la caja, el ánodo y el cátodo se sumergen en un disolvente orgánico (el éter es un solvente común) que actúa como electrolito, dentro del cual se coloca el separador. El separador es una lámina muy delgada de plástico microperforado. Como su nombre indica, separa los electrodos positivo y negativo, evitando cortocircuitos entre ambos; además permite que los iones pasen a través de sus microporos. Una primera diferencia entre las baterías ion-litio y las convencionales, es su mayor densidad energética, que alcanza valores del orden de 120 Wh/kg, tal y como muestra la siguiente imagen, donde se compara este factor para diversas tecnologías de baterías recargables existentes en la actualidad:
Densidad energética de las diversas tecnologías de baterías recargables, expresadas en términos volumétricos (eje vertical) y másicos (eje horizontal). Fuente: Yedukondalu Meesala, Anirudha Jena, Ho ChangRu-Shi Liu, Ru-Shi Liu, "Recent Advancements in Li-Ion Conductors for All-Solid-State Li-Ion Batteries", ACS Energy Letters, 2, 2734 (2017)
4. Aplicaciones de las baterías de ion-litio
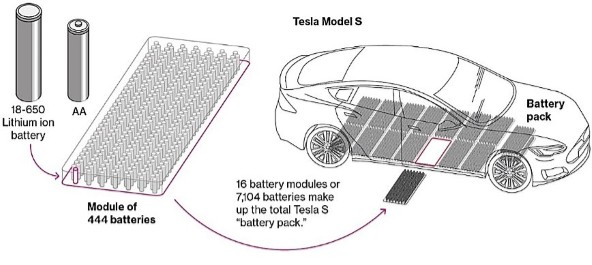
Como ya he indicado, una de las principales fuentes de crecimiento para este mercado son las baterías destinadas a los vehículos eléctricos. En esta aplicación, las celdas-pilas se agrupan entre sí con múltiples unidades para proporcionar la energía necesaria que permite el funcionamiento de un vehículo de gran autonomía, como se muestra en la siguiente imagen:
Esquema de la batería de un vehículo eléctrico, modelo Tesla S, construida a partir de la unión de más de 7000 pilas de ion-litio del modelo 18-650, muy similares en tamaño y forma a las clásicas AA. Están agrupadas en 16 módulos de 444 pilas. La batería en su conjunto pesa alrededor de 600 kg., aunque solo 7 kg. son de litio. Fuente de la figura: Jessica Shankleman, Tom Biesheuvel, Joe Ryan y Dave Merrill. Bloomberg Businessweek, 7-septiembre-2017
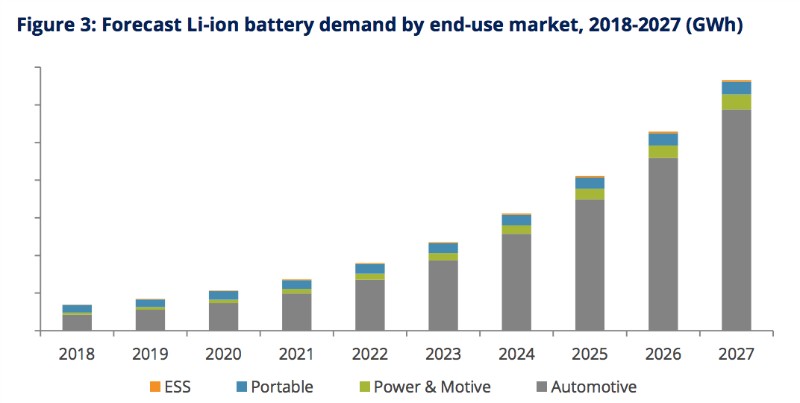
En la próxima década, está previsto un enorme incremento de la demanda de estas baterías, especialmente para su aplicación en vehículos eléctricos:
Previsiones de crecimiento del mercado de las baterías de ion-litio por sectores. Fuente: "Lithium demand will raise more than threefold by 2027". Tawaki, 20-julio-2018
En el próximo artículo de esta serie de dos, describiré con cierto detalle el funcionamiento de estas baterías.
Comentarios
<% if(canWriteComments) { %> <% } %>Comentarios:
<% if(_.allKeys(comments).length > 0) { %> <% _.each(comments, function(comment) { %>-
<% if(comment.user.image) { %>
![<%= comment.user.username %>]() <% } else { %>
<%= comment.user.firstLetter %>
<% } %>
<% } else { %>
<%= comment.user.firstLetter %>
<% } %>
<%= comment.user.username %>
<%= comment.published %>
<%= comment.dateTime %>
<%= comment.text %>
Responder
<% if(_.allKeys(comment.children.models).length > 0) { %>
<% }); %>
<% } else { %>
- No hay comentarios para esta noticia.
<% } %>
Mostrar más comentarios<% _.each(comment.children.models, function(children) { %> <% children = children.toJSON() %>-
<% if(children.user.image) { %>
![<%= children.user.username %>]() <% } else { %>
<%= children.user.firstLetter %>
<% } %>
<% } else { %>
<%= children.user.firstLetter %>
<% } %>
<% if(children.parent.id != comment.id) { %>
en respuesta a <%= children.parent.username %>
<% } %>
<%= children.user.username %>
<%= children.published %>
<%= children.dateTime %>
<%= children.text %>
Responder
<% }); %>
<% } %> <% if(canWriteComments) { %> <% } %>